
ОПРЕДЕЛЕНИЕ ТЕПЛОПОДНОСТИ ТОПЛИВА
11 декабря 2023 г.Steam, его создание и использование от Babcock & Компания Wilcox входит в серию книг HackerNoon. Вы можете перейти к любой главе этой книги здесь. ОПРЕДЕЛЕНИЕ ТЕПЛОтворной способности ТОПЛИВА
ОПРЕДЕЛЕНИЕ ТЕПЛОВОЙ СТОИМОСТИ ТОПЛИВА
Теплотворная способность топлива может быть определена либо путем расчета на основе химического анализа, либо путем сжигания образца в калориметре.
В первом методе расчет должен быть основан на окончательном анализе, который разлагает топливо на его элементарные составляющие: углерод, водород, кислород, азот, серу, золу и влагу, чтобы обеспечить разумную степень точности. Экспресс-анализ, определяющий только процентное содержание влаги, связанного углерода, летучих веществ и золы, без определения конечного состава летучих веществ, не может быть использован для расчета теплоты сгорания с той же степенью точности, что и окончательный анализ. но оценки могут быть основаны на окончательном анализе, который вполне верен.
Для окончательного анализа требуются услуги компетентного химика, а методы, которые следует использовать для такого определения, можно найти в любой стандартной книге по технической химии. Окончательный анализ, хотя и разделяет топливо на его элементарные составляющие, не показывает, как они могли быть объединены в топливе. Способ их сочетания, несомненно, оказывает прямое влияние на их теплотворную способность, так как топлива, имеющие почти одинаковые конечные анализы, при испытании в калориметре показывают разницу в теплотворной способности. Однако такая разница незначительна, и на основе окончательного анализа можно получить очень близкие приближения.
Окончательные анализы проводятся как для влажного, так и для сухого топлива. Поскольку последнее является общепринятой основой для сравнения данных, может показаться, что это лучшая основа для проведения такого анализа. Когда анализ проводится на влажной основе топлива, его можно легко перевести на сухую основу, разделив процентное содержание различных компонентов на единицу минус процент влаги, указав содержание влаги отдельно.
| | Влажное топливо | Сухое топливо | |----|----|----| | С | 83,95 | 84,45 | | Ч | 4.23 | 4,25 | | О | 3.02 | 3.04 | | Н | 1,27 | 1,28 | | С | .91 | .91 | | Эш | 6.03 | 6.07 | | | | ––––––––––– | | | | 100,00 | | Влага | .59 | .59 | | | ––––––––––– | | | | 100,00 | |
Расчеты на основе окончательного анализа. Первая формула для расчета теплотворной способности на основе состава топлива, определенного на основе окончательного анализа, принадлежит Дюлонгу, и эта формула, слегка измененная, в настоящее время наиболее часто используется. Были предложены и другие формулы, некоторые из которых более точны для определенных классов топлива, но все они основаны на формуле Дюлонга, принятая модифицированная форма которой такова:
Тепловые единицы в Б. т. ты. на фунт сухого топлива =
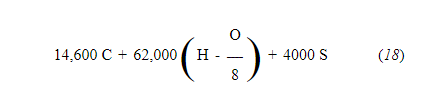
где C, H, O и S — пропорциональные весовые части углерода, водорода, кислорода и серы.
Предположим, что это уголь данного состава. Подставив в эту формулу (18),< /п>
Теплотворная способность фунта сухого угля
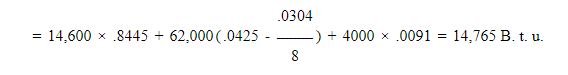
Этот уголь по калориметрическому тесту показал 14 843 Б.т. е., и при сравнении будет отмечена степень точности формулы.
Исследования Лорда и Хааса в этой стране, Маблера во Франции и Бунте в Германии показывают, что формула Дюлонга дает результаты, почти идентичные результатам, полученным в результате калориметрических испытаний, и может безопасно применяться ко всем твердым видам топлива, за исключением каменного угля, бурого угля и дерна. и древесина, при условии, что окончательный анализ верен. Это практически ограничивает его использование углем. Ограничивающими признаками являются наличие водорода и углерода, объединенных в форму углеводородов. Такие углеводороды присутствуют в углях в небольших количествах, но они имеют положительную и отрицательную теплоту соединения, и в углях они, по-видимому, компенсируют друг друга, что, безусловно, достаточно, чтобы применить формулу к таким топливам.
Высокая и низкая теплотворная способность топлива. В любом топливе, содержащем водород, теплотворная способность, определенная калориметром, выше, чем получаемая в большинстве условий работы в котельной практике, на величину, равную скрытой теплоте испарения воды. Это тепло снова появится при конденсации пара, хотя в обычной практике пар уходит несконденсированным. Этот факт приводит к различению теплотворной способности на так называемую «высшую» и «низшую» теплоту сгорания. Чем выше значение, i. э., определяемый калориметром, является единственной научной единицей, значением, которое следует использовать при испытаниях котлов, и рекомендованным Американским обществом инженеров-механиков.
Не существует абсолютной меры низшей теплоты сгорания, и ввиду большого расхождения во мнениях среди физиков относительно выводов, которые следует делать из высшей или абсолютной единицы при этом определении, низшую величину следует считать искусственной единицей. Более низкое значение влечет за собой использование окончательного анализа и предполагает допущения, которые сделают использование такого устройства невозможным для коммерческой работы. Использование низкого значения также может привести к ошибке и никоим образом не рекомендуется для использования в котлах.
Примером его нелогичного использования может служить рассмотрение котла, работающего со специальным экономайзером, в котором образующийся при водороде пар частично конденсируется экономайзером. Если при расчете эффективности котла использовалось низкое значение, то очевидно, что общий КПД комбинированного котла и экономайзера должен быть ошибочным, поскольку в счет этой комбинации учитывается теплота, передаваемая при конденсации пара, и не зачисляется такое тепло в теплотворную способность. угля.
Теплотворная способность газообразного топлива. Метод расчета теплотворной способности на основе окончательного анализа особенно адаптирован для твердого топлива, за уже отмеченными исключениями. Теплотворная способность газообразного топлива может быть рассчитана по формуле Дюлонга при условии добавления еще одного члена, учитывающего наличие угарного газа. Однако такой метод предполагает разделение составляющих газов на их элементарные газы, что часто является трудным и может привести к простой арифметической ошибке. Поскольку горючая часть газообразного топлива обычно состоит из водорода, окиси углерода и некоторых углеводородов, определение теплотворной способности гораздо легче получить путем разделения на составляющие их газы и расчета теплотворной способности по таблице таких значений. из составляющих. В Таблице 37 указана теплотворная способность наиболее распространенных горючих газов, а также теоретическое количество воздуха, необходимое для их сгорания.
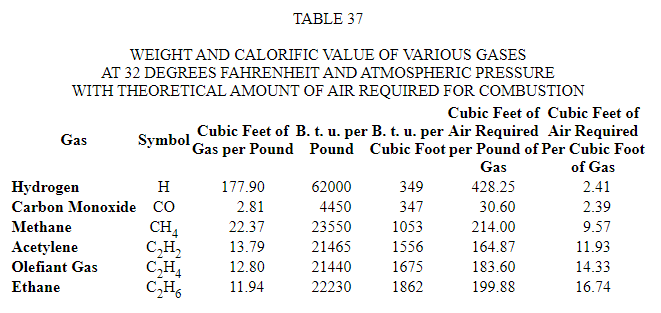
При применении этой таблицы, поскольку результаты анализа газов могут сообщаться либо по весу, либо по объему. , приведено в таблице 33[36] метод перехода от объемного анализа к анализу по весу.
Примеры:
1-й. Предположим, что это доменный газ, анализ которого в массовых процентах: кислород = 2,7, окись углерода = 19,5, диоксид углерода = 18,7, азот = 59,1. Здесь единственным горючим газом является окись углерода, а теплота сгорания будет равна,
| 0,195 | × | 4450 | = | 867,75 Б.т. ты. за фунт. | |----|----|----|----|----|
чистый объем воздуха, необходимый для сжигания одного фунта этого газа, составит
| 0,195 | × | 30,6 | = | 5,967 кубических футов. | |----|----|----|----|----|
2-й. Предположим, что это природный газ, анализ которого в объемных процентах: кислород = 0,40, окись углерода = 0,95, диоксид углерода = 0,34, олефиантный газ (C2H4) = 0,66, этан (C2H6) = 3,55, болотный газ (CH4) = 72,15. и водород = 21,95. Все, кроме кислорода и углекислого газа, являются горючими веществами, а количество тепла на кубический фут составит:
| От | СО | = | 0,0095 | × | 347 | = | 3.30 | |----|----|----|----|----|----|----|----| | | C2H4 | = | 0,0066 | × | 1675 | = | 11.05 | | | C2H6 | = | 0,0355 | × | 1862 | = | 66,10 | | | CH4 | = | 0,7215 | × | 1050 | = | 757,58 | | | Ч | = | 0,2195 | × | 349 | = | 76,61 | | ––––––––––– | | | | | | | | | | | | | | Б. т. ты. за кубический фут | = | 914,64 |
чистый воздух, необходимый для сгорания одного кубического фута газа, составит:
| СО | = | 0,0095 | × | 2,39 | = | 0,02 | |----|----|----|----|----|----|----| | C2H4 | = | 0,0066 | × | 14.33 | = | 0,09 | | C2H6 | = | 0,0355 | × | 16,74 | = | 0,59 | | CH4 | = | 0,7215 | × | 9,57 | = | 6,90 | | Ч | = | 0,2195 | × | 2.41 | = | 0,53 | | ––––––– | | | | | | | | | | | | Общий чистый воздух на кубический фут | = | 8.13 |
Приблизительный анализ. Приблизительный анализ топлива позволяет определить его весовые пропорции связанного углерода, летучих горючих веществ, влаги и золы. Ниже описан метод проведения такого анализа, который, как было установлено, дает весьма удовлетворительные результаты.
Из пробы угля, полученной при испытании котла, раздробляют и взвешивают среднюю пробу массой около 40 граммов. Хорошим средством сокращения такого образца является пропускание его через обычную кофемолку. Этот образец следует поместить в воздушную баню с двойными стенками, в которой следует поддерживать примерно постоянную температуру 105 градусов по Цельсию, при этом образец периодически взвешивают до тех пор, пока не будет достигнут минимум. Процент влаги можно рассчитать по потерям при такой сушке.
Для определения остатка анализа и теплотворной способности топлива часть этой высушенной пробы следует тщательно измельчить и, если ее предполагается сохранить, поместить в герметичный сосуд. Один грамм измельченной пробы следует взвесить в фарфоровом тигле с хорошо закрывающейся крышкой. Этот тигель следует поставить на платиновый треугольник и нагревать в течение семи минут на полном пламени бунзеновской горелки. По истечении этого времени пробу следует поместить в эксикатор, содержащий хлорид кальция, и после охлаждения взвесить. По потерям можно легко рассчитать процент летучих горючих веществ.
Для определения процентного содержания золы следует использовать ту же пробу, из которой были выделены летучие вещества. Этот процент получают сжиганием связанного углерода на горелке Бунзена или в муфельной печи. Горение следует поддерживать до тех пор, пока не будет достигнут постоянный вес; этому можно способствовать помешиванием платиновой палочкой. Вес остатка определяет процент золы, а процент связанного углерода легко рассчитывается по потерям при определении золы после удаления летучих веществ.
Экспресс-анализы могут быть выполнены и представлены на влажной или сухой основе. Сухая основа — это общепринятая основа, и именно она принята в этой книге. Метод перевода влажной основы в сухую аналогичен описанному в случае окончательного анализа. Экспресс-анализ легко проводится и дает информацию об общих характеристиках топлива и его относительной теплотворной способности.
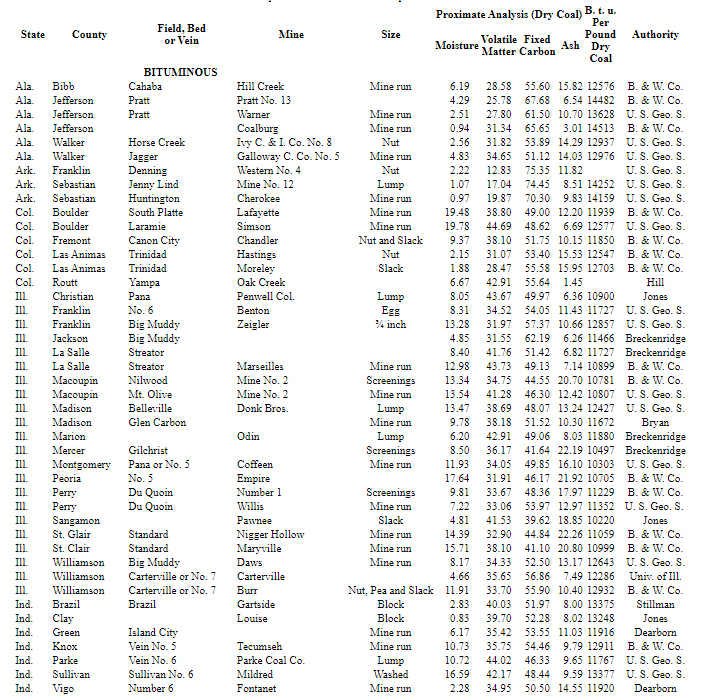
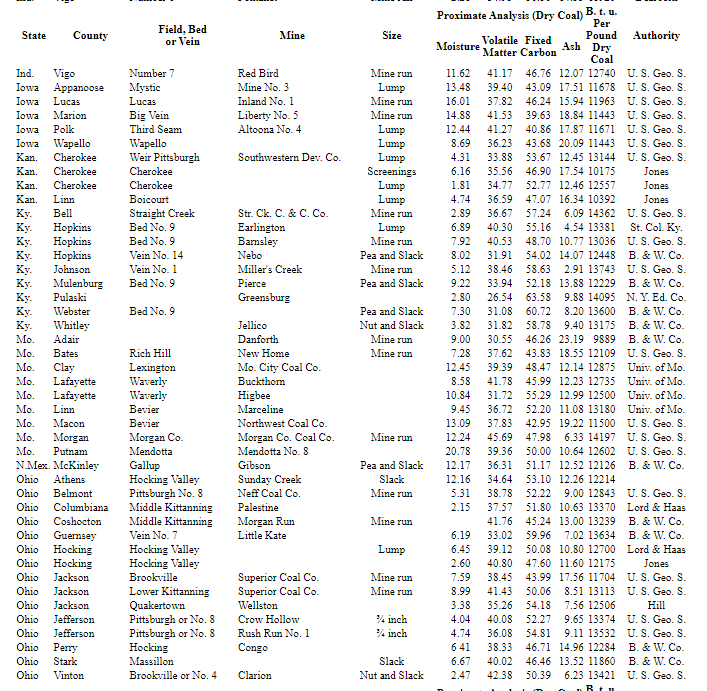
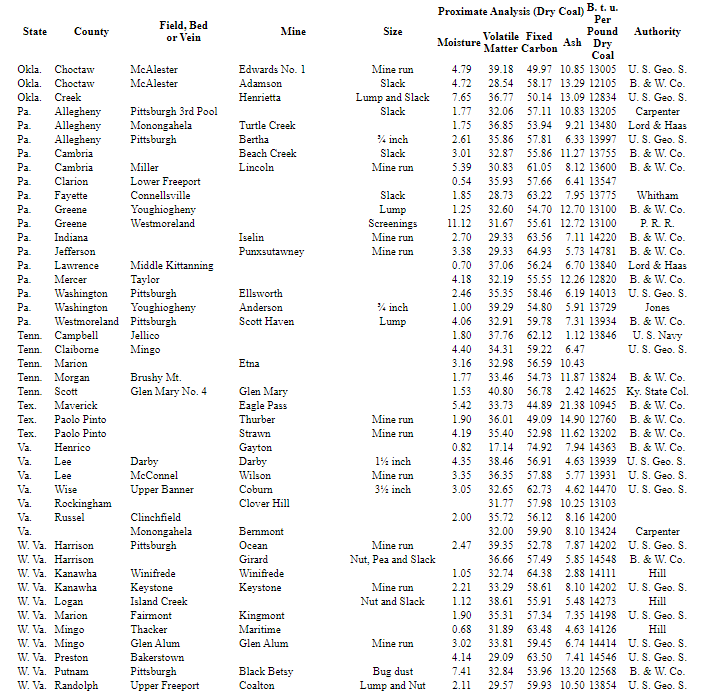
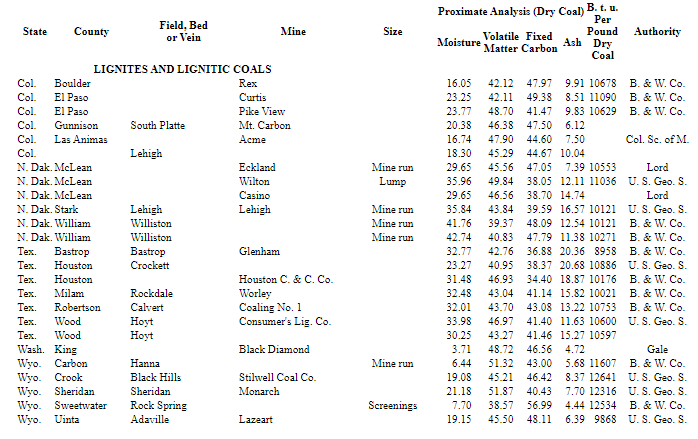
В Таблице 38 приведены приблизительный анализ и теплотворная способность ряда обнаруженных репрезентативных углей. в США.
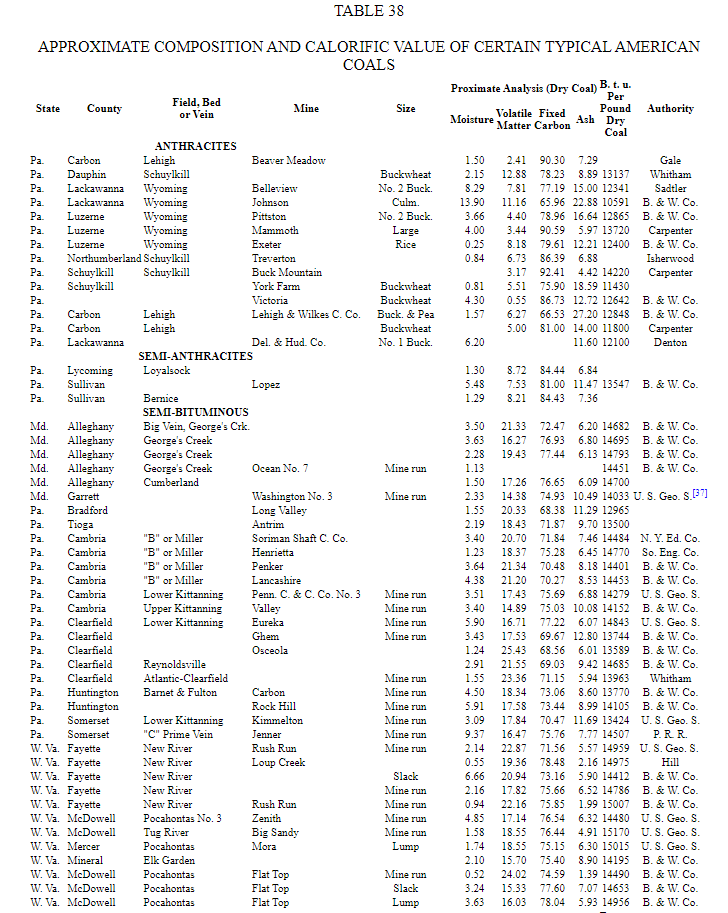

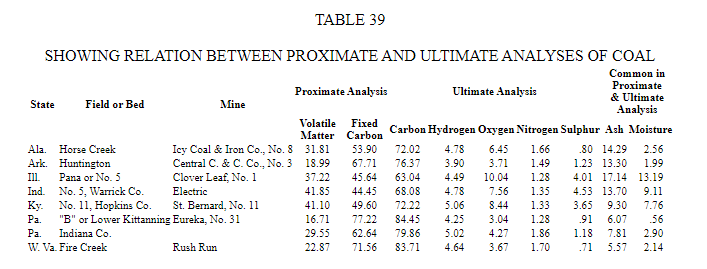
В Таблице 39 для сравнения приведены окончательные и приблизительные анализы некоторых углей с какие испытания проводились на испытательном стенде Геологической службы США на выставке закупок Луизианы в Сент-Луисе.
Теплотворная способность топлива не может быть рассчитана непосредственно на основе приближенного анализа из-за того, что содержание летучих веществ широко варьируется в различных топливах по составу и теплотворной способности.
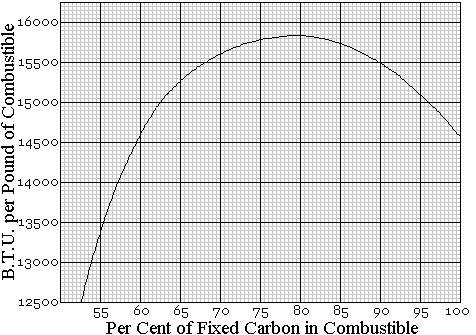
Разработаны некоторые методы оценки теплотворной способности углей на основе экспресс-анализа. Уильям Кент[38] вывел из испытаний Малера европейских углей приблизительную теплотворную способность зависит от содержания связанного углерода в горючем топливе. Зависимость, выведенная Кентом, между теплотой и ценностью фунта горючего и процентом связанного углерода, относящегося к горючему, графически представлена на рис. 23.
Гуталь приводит другой метод определения теплотворной способности на основе экспресс-анализа, в котором углероду придается фиксированное значение, а теплотворная способность летучего вещества рассматривается как функция его процентного содержания, отнесенного к горючему веществу. Метод Гуталя тесно связан с определениями Кента.
Однако все формулы для расчета теплотворной способности углей на основе точного анализа обычно ограничиваются определенными классами топлива. Г-н Кент, например, утверждает, что его выводы верны в близких пределах для топлива, содержащего более 60 процентов связанного углерода в горючем топливе, в то время как для топлива, содержащего более низкий процент, ошибка может достигать 4 процентов. , либо высокий, либо низкий.
Хотя использование таких вычислений будет полезно там, где требуются только приблизительные результаты, следует полностью понимать, что они являются приблизительными.
Калориметрия. Окончательный или приблизительный анализ топлива полезен для определения его общих характеристик, как описано на странице 183 может использоваться при расчете приблизительной теплотворной способности. Однако если необходимо рассчитать эффективность котла, эта теплотворная способность во всех случаях должна определяться точно с помощью топливного калориметра.
В таком аппарате топливо полностью сгорает, а тепло, образующееся при таком сгорании, поглощается водой, причем количество тепла рассчитывается по повышению температуры воды. Лучшим для таких работ признан калориметр, в котором топливо сжигается в стальной бомбе, наполненной сжатым кислородом. Функция кислорода, который обычно находится под давлением около 25 атмосфер, заключается в том, чтобы вызвать быстрое и полное сгорание образца топлива. Топливо воспламеняется посредством электрического тока с учетом выделяемого этим током тепла и горения плавкой проволоки.
Калориметр этого типа, который, как будет установлено, дает удовлетворительные результаты, - это калориметр М. Пьера Малера, показанный на рис. 24 и состоящий из следующих частей:
Водяная рубашка A, которая поддерживает постоянные условия за пределами самого калориметра и, таким образом, позволяет более точно рассчитывать потери на радиацию.
Стальная бомба с фарфоровой облицовкой B, в которой горение топлива происходит в сжатом кислороде.
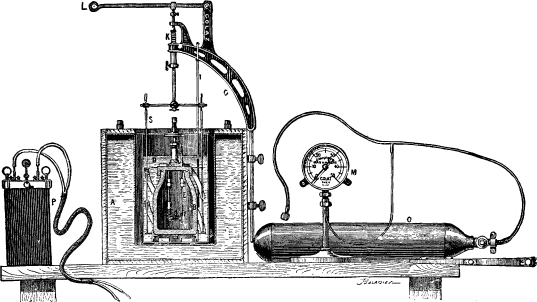
Платиновый поддон C для хранения топлива.
Собственно калориметр D, окружающий бомбу и содержащий определенную навеску воды.
Электрод E, соединенный с плавким проводом F, для воспламенения топлива, помещенного в поддон C.
Опора G для мешалки для воды.
Термометр I, для определения температуры воды в калориметре. Термометр лучше всего поддерживать на независимой от калориметра подставке, чтобы он не мог смещаться из-за сотрясений частей калориметра, что затруднило бы получение показаний. Для получения точности показаний их следует снимать через телескоп или окуляр.
Пружинно-винтовое устройство для вращения мешалки.
Рычаг L, движением которого вращается мешалка.
Манометр M для измерения количества кислорода, поступившего в бомбу. Обычно используется от 20 до 25 атмосфер.
Кислородный баллон O.
Батарея или батареи P, ток от которых нагревает плавкий провод, используемый для воспламенения топлива.
Этот или аналогичный калориметр используется для определения теплоты сгорания твердого или жидкого топлива. Какое бы топливо ни было испытано, нельзя придавать слишком большое значение обеспечению среднего образца. При испытании угля испытания следует проводить на части высушенной и измельченной лабораторной пробы, способы получения которой описаны. При рассмотрении методов калориметрического определения замечания, примененные к углю, в равной степени применимы и к любому твердому топливу, а такие изменения в методах, которые необходимы для жидких топлив, будут самоочевидны из того же описания.
Примерно один грамм измельченной высушенной пробы угля следует поместить непосредственно в чашку калориметра. Существует некоторая опасность в использовании измельченного образца, поскольку часть его может вылететь из чаши при поступлении кислорода. Эту проблему можно, по крайней мере частично, преодолеть, формируя брикет из примерно двух граммов с помощью цилиндра, оснащенного плунжером, и шнекового пресса. Такой брикет следует разломать и использовать примерно один грамм. Если используется измельченный образец, следует позаботиться о том, чтобы кислород впускался медленно, чтобы не допустить выдувания угля из поддона. Вес образца ограничен примерно одним граммом, поскольку калориметр рассчитан на сжигание примерно этого веса при давлении кислорода около 25 атмосфер.
К нижнему концу плунжера подсоединен кусок тонкой железной проволоки, образующий предохранитель для воспламенения образца. Определяют вес использованной железной проволоки, и если после сгорания часть не сгорела, определяют вес такой части. При помещении образца в чашку и регулировке предохранителя верхнюю часть калориметра снимают. Затем его заменяют на место и осторожно прикручивают к бомбе с помощью гаечного ключа с длинной ручкой, предназначенного для этой цели.
Затем бомбу помещают в калориметр, наполненный определенным количеством воды. Этот вес является «водным эквивалентом» аппарата, т.е. е., вес воды, температура которой увеличилась бы на один градус для эквивалентного повышения температуры комбинированного аппарата. Ее можно определить расчетным путем, исходя из массы и удельной теплоемкости различных частей аппарата. Однако такое определение может быть ошибочным, поскольку вес обшивки бомбы можно оценить лишь приблизительно, а значительная часть устройства не погружена в воду. Другой метод такого определения состоит в добавлении определенных навесок теплой воды к определенным количествам более холодной воды в калориметре и усреднении результатов ряда экспериментов. Лучшим методом такого определения, вероятно, является сжигание определенного количества ресублимированного нафталина, теплота сгорания которого известна.
Температура воды в водяной рубашке калориметра должна быть примерно равна температуре окружающей атмосферы. Температуру навески воды в калориметре некоторые экспериментаторы делают несколько большей, чем температура окружающего воздуха, чтобы первоначальная поправка на излучение была в том же направлении, что и конечная поправка. Другие экспериментаторы начинают с температуры, равной или немного ниже температуры помещения, исходя из того, что температура после горения будет немного выше комнатной и радиационная поправка будет либо минимальной, либо полностью исключенной.
Хотя экспериментов, которые бы убедительно показали, какой из этих методов лучше, не проводилось, обычно используется последний.
После помещения бомбы в калориметр ее наполняют кислородом из баллона до достижения давления от 20 до 25 атмосфер. Более низкого давления будет достаточно во всех случаях, кроме исключительных. Затем подключают ток от сухих батарей последовательно, расположенных так, чтобы можно было завершить цепь переключателем. Для воспламенения не следует использовать ток от системы освещения, так как при сгорании предохранителя существует опасность искрения, которое может повлиять на результаты. После этого устройство готово к тестированию.
Несомненно, лучший метод получения данных — это использование координатной бумаги и отображение данных с температурой и временными интервалами в виде ординат и абсцисс. Такое графическое представление показано на рис. 25.
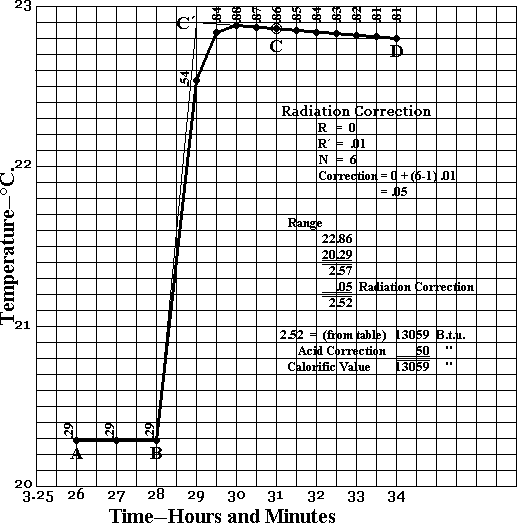
После помещения бомбы в калориметр и до воспламенения угля следует снимать показания температуры воды с интервалом в одну минуту в течение периода, достаточно длительного, чтобы обеспечить постоянную скорость изменения, и таким образом определить начальную температуру воды. радиация. Затем уголь воспламеняется при замыкании контура, при этом температура в момент замыкания контура считается температурой в начале горения. После зажигания показания следует снимать с интервалом в полминуты, однако из-за быстроты подъема ртути приблизительные показания могут быть возможны только в течение, по крайней мере, минуты после зажигания, однако такие показания являются достаточно точными для этого периода. Полуминутные показания следует снимать после зажигания в течение пяти минут и, скажем, еще пять минут с минутными интервалами, чтобы точно определить окончательную скорость излучения.
На рис. 25 показаны результаты таких показаний, построенные в соответствии с предложенной методикой. Теперь осталось вычислить результаты на основе этих построенных данных.
Сначала применяется радиационная коррекция. Вероятно, наиболее точным способом такой коррекции является использование метода Пфаундлера, который является модификацией метода Реньо. Это предполагает, что, начиная с начальной скорости излучения, представленной наклоном линии AB, рис. 25, и заканчивая конечным излучением, представленным наклоном линии CD , рис. 25, видно, что скорости излучения для промежуточных температур между точками B и C пропорциональны начальной и конечной скоростям. То есть скорость излучения в точке посередине между B и C будет средним между начальной и конечной скоростью; уровень радиации в точке, находящейся на расстоянии трех четвертей расстояния между B и C, будет равен уровню в B плюс три четверти расстояния разница в скоростях при B и C и т. д. Этот метод отличается от метода Реньо тем, что Реньо предполагал, что излучение в каждом случае пропорционально разнице температур между воды калориметра и окружающего воздуха плюс константа, найденная для каждого опыта. Метод Пфаундлера проще, чем метод Реньо, и результаты обоих методов практически согласуются.
Выраженный в виде формулы метод Пфаундлера, хотя и не в данной им форме, таков:

Применение этой формулы к рис. 25 выглядит следующим образом:
Как уже говорилось, температура в начале горения — это значение непосредственно перед включением тока, или B на рис. 25. Точка C или температура при сгорание которого предположительно завершилось, следует принимать в точке, которая находится в пределах установленной конечной скорости излучения, а не при максимальной температуре, которую показывает термометр при испытании, если только она не лежит на прямой линии, определяющей конечное излучение. Это связано с тем, что в некоторых случаях местные условия заставят показания термометра выше, чем должны, в то время, когда бомба быстро передает тепло воде, а в других случаях максимальная температура может быть ниже той, которая была бы следует указать, если показания следует снимать с интервалом менее половины минуты, i. е., точка максимальной температуры опустится ниже линии, определяемой конечной скоростью излучения. При таком понимании AB, рис. 25, представляет время начального излучения, BC — время горения, а CD — время окончательного излучения. . Поэтому, чтобы применить поправку Пфаундлера, формула (19 ), к данным, представленным на рис. 25.
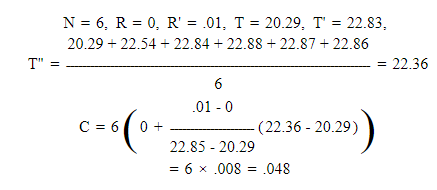
Формула Пфаундлера, хотя и проста, но довольно длинна. Г-н Э. Х. Пибоди разработал более простую формулу, с помощью которой при надлежащих условиях отклонение от поправки, найденной методом Пфаундлера, незначительно.
В ходе расширенной серии испытаний калориметра было отмечено, что максимальная температура термометра была достигнута чуть более чем через одну минуту после обжига. Если бы этот период между временем обжига и зарегистрированной максимальной температурой составлял ровно одну минуту, радиация за этот период была бы равна радиации за полминуты до обжига плюс радиация за полминуты < em>после достижения максимальной температуры; или излучение за минутный интервал будет представлять собой среднее значение излучения в минуту до срабатывания и излучения в минуту после максимума. Построенная диаграмма температур будет иметь вид кривой из трех прямых линий (B, C', D) на рис. 25. В таких условиях используются обозначения формулы (19< /em>) исправление будет выглядеть следующим образом:
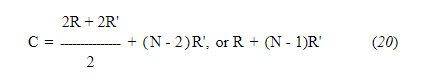
Эту формулу можно обобщить для условий, когда максимальная температура достигается через период более одной минуты, следующим образом:
Пусть М = количество интервалов между временем обжига и максимальной температурой. Тогда излучение за этот период будет средним значением излучения за М интервалов до выстрела и за М интервалов после регистрации максимума, или
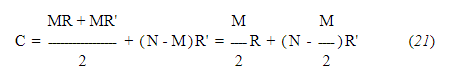
В случае выводов г-на Пибоди M оказалось равным примерно 2 и формуле (21) становится напрямую, C = R + (N - 1)R' или формулой (20).
Вносимые поправки, обеспечиваемые применением этой формулы, очень близки к поправкам, получаемым по методу Пфаундлера, где точка максимальной температуры находится не более чем на пять интервалов позже точки обжига. Если на графике температур указан более длительный период, то приближенную формулу использовать не следует. По мере увеличения периода между обжигом и максимальной температурой полученные результаты все дальше и дальше отходят от теоретической прямой кривой. Если этот период не превышает пяти интервалов или двух с половиной минут, аппроксимацию прямой кривой можно построить на глаз, и обычно применяемую радиационную поправку можно очень точно определить по такой аппроксимированной кривой.
Приблизительная формула Пибоди была найдена в результате ряда испытаний и дает результаты в пределах 0,003 градуса по Фаренгейту в пределах, в которых ее применение справедливо, как описано. Значение M, которое не обязательно является целым числом, должно определяться для каждого испытания, хотя, по всей вероятности, такое значение является константой для любого отдельного калориметра, который правильно эксплуатируется.
Во всех случаях необходимо добавить поправку на радиацию, приведенную на странице 188. к диапазону температур между точкой воспламенения и выбранной точкой, от которой рассчитывается окончательное излучение. Этот скорректированный диапазон, умноженный на водный эквивалент калориметра, дает теплоту сгорания в калориях угля, сожженного в калориметре, вместе с теплотой, выделяемой при сгорании плавкой проволоки. Теплоту, выделяемую при сгорании плавкой проволоки, определяют путем определения фактического веса сгоревшей проволоки и теплоты сгорания одного миллиграмма проволоки (1,7 калории), i. е., умножьте вес используемой проволоки на 1,7, и результат будет выражен в граммах калорий или количестве тепла, необходимого для поднятия одного грамма воды на один градус Цельсия.
Другие небольшие поправки, которые необходимо сделать, касаются образования азотной кислоты и сжигания серы в серную кислоту вместо диоксида серы из-за более полного сгорания в присутствии кислорода, чем это было бы возможно в атмосфере.
Для внесения этих поправок бомбу калориметра после каждого испытания тщательно промывают водой и определяют количество кислоты, титрованием этой воды стандартным раствором аммиака или каустической соды, причем всю кислоту принимают за азотную. Каждый кубический сантиметр использованного раствора для титрования аммиака эквивалентен поправке на 2,65 калории.
Поскольку часть кислотности обусловлена образованием серной кислоты, необходима дальнейшая коррекция. При сжигании серной кислоты теплота, выделяемая на грамм серы, на 2230 калорий превышает тепло, которое выделилось бы, если бы сера сгорела до диоксида серы, или 22,3 калории на каждый процент серы в угле. Один кубический сантиметр раствора аммиака эквивалентен 0,00286 грамма серы в виде серной кислоты, или 0,286 × 22,3 = 6,38 калорий. Очевидно поэтому, что после умножения количества кубических сантиметров, использованных при титровании, на тепловой коэффициент азотной кислоты (2,65), необходима дополнительная поправка 6,38 — 2,65 = 3,73 на каждый кубический сантиметр, использованный при титровании серной вместо азотной кислоты. Эта поправка составит 3,73/0,297 = 13 единиц на каждые 0,01 грамма серы в угле.
Таким образом, общая поправка на водные растворы азотной и серной кислоты находится путем умножения количества аммиака на 2,65 и добавления 13 калорий на каждые 0,01 грамма серы в угле. Эта общая поправка должна быть вычтена из значения теплоты, полученного из скорректированного диапазона, и количества, эквивалентного калориметру.
После каждого испытания необходимо тщательно осмотреть поддон, в котором сгорел уголь, чтобы убедиться, что весь образец полностью сгорел. Наличие черных пятен обычно указывает на несгоревший уголь, и их часто можно обнаружить там, где уголь содержит кость или сланец. При обнаружении таких пятен испытания следует повторить. При испытании любого топлива, когда трудно полностью израсходовать образец, можно добавить навеску нафталина, при этом общий вес топлива и нафталина составляет примерно один грамм. Нафталин имеет известную теплоту сгорания, образцы для этой цели можно получить в Бюро стандартов США, а по совокупной теплоте сгорания топлива и нафталина можно легко рассчитать теплоту сгорания первого.
Теплоту, выделяющуюся при горении определенной массы стандартного нафталина, можно использовать и как средство калибровки калориметра в целом.
О книжной серии HackerNoon: мы предлагаем вам наиболее важные технические, научные и познавательные книги, являющиеся общественным достоянием.
Эта книга является общественным достоянием. Бэбкок и amp; Компания Уилкокс (2007). Steam, его создание и использование. Урбана, Иллинойс: Проект Гутенберг. Получено https://www.gutenberg.org/cache/epub/22657/pg22657-images.html.
Эта электронная книга предназначена для использования кем угодно и где угодно, бесплатно и практически без каких-либо ограничений. Вы можете скопировать ее, отдать или повторно использовать в соответствии с условиями лицензии Project Gutenberg, включенной в данную электронную книгу или на сайте www.gutenberg.org< /a>, расположенный по адресу https://www.gutenberg.org/policy/license.html.. эм>
Оригинал
